导语:
2026年1月,北京中医药大学研究团队在《Journal of Experimental & Clinical Cancer Research》发表题为《Disruption of HSPA8-GEMIN5 interaction suppresses colorectal cancer by impaired splicing-translation coupling-mediated proteostasis imbalance》的研究,系统解析了天然化合物去氧紫草素(Deoxyshikonin, DSHK)的抗结直肠癌(CRC)作用及分子机制,首次揭示HSPA8-GEMIN5复合物作为“剪接-翻译偶联”分子枢纽的关键功能,提出“靶向剪接与翻译双通路”的CRC治疗新策略。
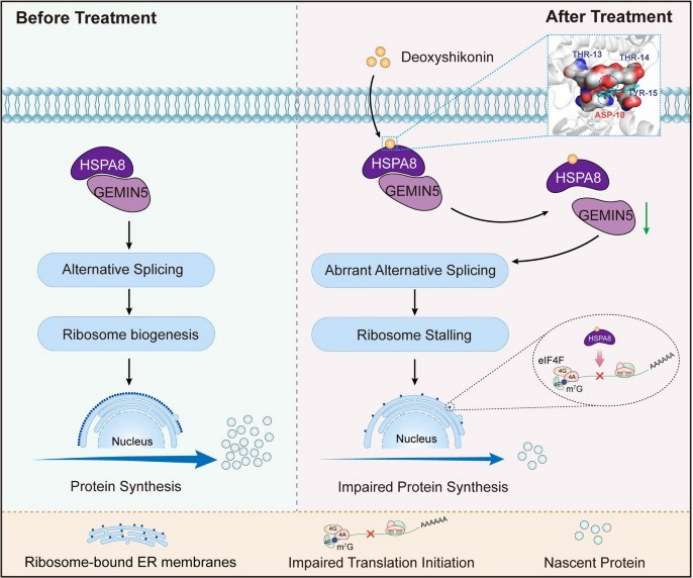
本研究创新性应用SPIDER邻近标记技术、蛋白质组学等多维度技术,明确DSHK的直接靶点为HSPA8,并阐明其通过破坏HSPA8-GEMIN5相互作用,同步诱导核糖体蛋白编码基因异常剪接与翻译起始功能障碍,最终引发蛋白稳态失衡的核心机制。研究在细胞系、患者来源类器官(PDO)及异种移植瘤(CDX/PDOX)模型中充分验证了DSHK的抗肿瘤活性及安全性,为CRC精准治疗提供了全新候选药物与作用靶点。
结直肠癌是全球发病率最高的恶性肿瘤之一,其恶性进展的核心驱动因素之一是肿瘤细胞通过异常蛋白合成重编程蛋白稳态。目前临床常用的核糖体靶向药物(如CX-5461)因对肿瘤特异性翻译通路的调控精准性不足,在实体瘤治疗中疗效有限。因此,阐明CRC中蛋白合成依赖的分子枢纽,开发选择性干预策略是该领域亟待解决的关键问题。
热休克蛋白HSPA8(HSP70家族核心成员)与RNA结合蛋白GEMIN5(SMN复合物组分)分别在翻译起始调控与前体mRNA剪接中发挥重要作用,但二者在肿瘤中的相互作用及协同调控机制尚未被探索。天然化合物DSHK已被证实具有潜在抗肿瘤活性,但其抗CRC的直接靶点与下游调控网络仍不明确,限制了其临床转化应用。
技术路线
1. DSHK抗CRC活性验证:体外(CRC细胞系、PDO)与体内(CDX、PDOX)模型系统性评估。
2. 靶点鉴定与验证:化学蛋白质组学、CETSA、SPR、分子动力学模拟锁定并验证HSPA8为DSHK直接靶点。
3. 互作蛋白筛选:SPIDER邻近标记技术鉴定HSPA8的新型功能互作蛋白GEMIN5。
4. 分子机制解析:多组学(转录组、可变剪接分析)与细胞生物学实验阐明“剪接-翻译偶联”紊乱机制。
5. 临床相关性验证:高密度组织芯片(TMA)分析HSPA8/GEMIN5在CRC组织中的表达与共定位特征。
主要结果
1.DSHK在临床前模型中展现强效抗CRC活性
研究团队采用“毒性-疗效”双维度评估框架,在7种人CRC细胞系(HCT-116、RKO、SW480等)、患者来源类器官(PDO)、细胞系来源异种移植(CDX)及患者来源类器官异种移植(PDOX)模型中系统验证了DSHK的抗CRC活性。结果显示,DSHK对正常结肠上皮细胞NCM460的48小时IC₅₀超过40μM,而对CRC细胞系的IC₅₀均低于5μM,其中SW480和DLD-1细胞对其最敏感(IC₅₀分别为1.59μM和1.34μM),体现出良好的肿瘤选择性毒性。在体内模型中,高剂量DSHK(5mg/kg)对CDX和PDOX模型的肿瘤抑制率分别达64.36%和70.32%,且未引发明显脏器毒性,同时显著下调增殖标志物Ki67、PCNA的表达,上调凋亡标志物cleaved-caspase3水平,证实其在体内的强效抗肿瘤作用。
2.HSPA8是DSHK抗CRC的直接分子靶点
通过化学蛋白质组学、细胞热位移分析(CETSA)、表面等离子体共振(SPR)及分子动力学模拟等多技术联合筛选,研究鉴定出HSPA8(HSP70家族核心成员)是DSHK的直接作用靶点。分子对接显示,DSHK与HSPA8的ASP10、THR13、THR14和TYR15残基形成氢键网络,其中ASP10是核心结合位点,单点突变(D10A)可完全阻断两者相互作用。SPR实验证实DSHK与HSPA8的结合常数KD为27.9μM,具有特异性结合能力。TCGA数据库分析显示,CRC组织中HSPA8mRNA表达显著高于癌旁正常组织,且高表达HSPA8的CRC患者总生存期显著缩短,提示其临床相关性。功能验证表明,通过siRNA或shRNA敲低HSPA8后,DSHK对CRC细胞增殖的抑制作用及体内抗肿瘤活性均显著减弱,证实DSHK的抗CRC效应依赖于HSPA8。
3.基于SPIDER技术鉴定HSPA8在CRC中的新型功能互作蛋白GEMIN5
为精准捕获HSPA8的功能性互作蛋白,研究团队创新性地采用SPIDER(Specific Pupylation as IDEntity Reporter)邻近标记技术,结合共价生物素标记策略,建立了高特异性的HSPA8互作组筛选体系。实验流程如下:将生物素化的HSPA8蛋白与CRC细胞裂解液共孵育后,加入SA-Pup4标记酶、ATP及PafA,在37℃下反应激活生物素化过程,使HSPA8邻近的互作蛋白被特异性标记;随后通过链霉亲和素琼脂糖珠捕获生物素化蛋白复合物,经胰酶消化后进行质谱分析。通过严格的筛选标准(≥2个独特肽段、生物学重复中Foldchange≥1.2),并排除核糖体蛋白、角蛋白等常见污染蛋白,最终鉴定出CHTOP、GEMIN5、H1-0及ACADVL四个高置信度的HSPA8共价结合蛋白。
进一步的分子动力学模拟显示,HSPA8-GEMIN5复合物具有高度结构稳定性(RMSD波动<0.4nm),两者通过三个关键氢键及静电互补作用形成紧密结合的纳米级复合物。TCGA数据库分析显示,GEMIN5在CRC组织中高表达,且与肿瘤增殖呈正相关,可作为不良预后预测指标。HSPA8敲低实验表明,HSPA8能显著延长GEMIN5蛋白半衰期,提示其对GEMIN5的稳定性调控作用。高分辨率组织芯片及多重免疫荧光分析证实,CRC组织中HSPA8与GEMIN5的表达水平及共定位强度均显著高于癌旁组织,且在肿瘤上皮细胞中选择性富集,为靶向干预提供了空间特异性基础。SPIDER技术的应用,突破了传统互作蛋白筛选技术的局限性,实现了对HSPA8功能性互作网络的精准捕获,为GEMIN5这一新型互作蛋白的发现提供了关键技术支撑。
4.DSHK破坏HSPA8-GEMIN5相互作用,引发双重分子紊乱
Co-IP及共聚焦显微镜分析显示,DSHK可浓度依赖性地削弱HSPA8与GEMIN5的结合亲和力,降低两者在CRC细胞、类器官及异种移植肿瘤组织中的共定位水平(Pearson相关系数显著下降)。机制研究表明,这种相互作用的破坏会引发两条关键通路紊乱:一方面,GEMIN5功能受损导致核糖体蛋白(RP)编码基因(RPL11、RPS14等)异常可变剪接,主要涉及可变3’剪接位点(A3SS)和可变5’剪接位点(A5SS),进而阻碍功能性核糖体生物发生,表现为粗面内质网核糖体密度降低、80S成熟核糖体峰减弱及40S/60S亚基比例失衡;另一方面,HSPA8介导的翻译起始因子相互作用受损,导致eIF4F复合物解离,翻译起始功能紊乱,最终共同抑制蛋白合成。
总结与展望
研究意义
该研究首次揭示了HSPA8-GEMIN5复合物在CRC“剪接-翻译偶联”中的核心调控作用,突破了传统分子伴侣仅参与蛋白折叠的认知,拓展了HSP70家族的功能范式。尤为重要的是,SPIDER邻近标记技术的成功应用,为肿瘤相关蛋白互作网络的解析提供了高特异性、高可信度的技术范例,解决了传统互作筛选中假阳性率高、弱相互作用难以捕获的技术瓶颈。DSHK作为首个靶向“剪接-翻译偶联”轴的天然化合物,通过双重通路干预实现CRC抑制,相比传统单一机制核糖体靶向药物,更能有效规避治疗耐药,为实体瘤治疗提供了新思路。同时,该研究建立的“活性-机制-临床验证”三维评价体系,为天然产物的抗肿瘤药物研发提供了可靠范式。
局限性
1. DSHK作为小分子抑制剂,体内药代动力学特性可能限制其对HSPA8功能的持续完全抑制,导致其单药疗效弱于HSPA8特异性敲低;
2. 目前尚未明确HSPA8-GEMIN5复合物识别RP前体mRNA的空间识别密码,需进一步通过冷冻电镜解析复合物与RNA的动态结合构象;
3. DSHK的肿瘤微环境穿透效率仍需优化,其在临床转化中的给药方式及联合治疗策略有待探索;
4. SPIDER技术虽实现了互作蛋白的高效捕获,但对于瞬时性、低亲和力的互作事件仍可能存在遗漏,未来可结合单细胞SPIDER技术进一步提升检测灵敏度。
拓展方向
未来可基于HSPA8-GEMIN5相互作用界面的结构特征,设计高特异性变构抑制剂,规避传统HSP70抑制剂的系统性毒性;通过整合RP编码基因的可变剪接图谱,筛选具有“剪接脆弱性”的CRC患者亚群,实现DSHK的精准临床应用。此外,开发靶向HSPA8的pH响应型纳米载体,可提高药物在肿瘤组织的富集效率;结合单细胞追踪技术与SPIDER邻近标记技术,实时监测核糖体组装动态及蛋白互作网络变化,可为“剪接依赖型蛋白稳态失衡”提供动力学证据,进一步推动CRC精准治疗的发展。
该研究不仅深化了对CRC蛋白合成调控网络的理解,更为天然化合物的抗肿瘤机制研究及临床转化提供了重要理论依据,同时也彰显了新型邻近标记技术在解析肿瘤分子调控网络中的关键作用,有望为CRC患者带来全新治疗选择。
WangF.,HuangH.,ZhangR.etal.DisruptionofHSPA8-GEMIN5interactionsuppressescolorectalcancerbyimpairedsplicing-translationcoupling-mediatedproteostasisimbalance.JExpClinCancerRes(2026).