导语:儿童哮喘是美国主要的公共卫生问题,每12名学龄儿童中就有1例患病。流行病学研究发现,来自低收入国家的移民母亲其后代哮喘风险显著更低,但背后的免疫机制长期不明。胎盘转运的母体IgG抗体是新生儿出生后早期被动免疫的主要来源,而母亲早年的微生物暴露可能塑造其抗体谱特征。噬菌体免疫沉淀测序(PhIP-seq)技术的出现,为高通量解析脐血中数千种微生物特异性抗体谱提供了可能。2026年,约翰霍普金斯大学等多机构联合团队在Allergy杂志发表重磅研究,首次在大规模前瞻性出生队列中揭示了母亲出生地、胎盘转运抗菌IgG抗体与儿童哮喘风险的三角关系,为儿童哮喘的病因学研究和预防策略提供了全新视角。
【发表期刊】Allergy(IF 12.6)
【发布时间】2026年1月
【主要技术】PhIP-seq(噬菌体免疫沉淀测序)
研究背景
儿童哮喘的发病机制复杂,遗传易感性、感染、环境因素及其相互作用均参与其中。尽管研究进展显著,但发达国家哮喘患病率仍持续上升。既往研究发现,来自低收入国家的移民及其美国出生的后代哮喘风险更低,推测与母亲早年暴露于多样化微生物环境相关——这种暴露可能塑造母体免疫系统,通过胎盘转运抗体影响子代免疫发育。
由于新生儿出生后4-6个月内自身IgG合成能力极弱,完全依赖母体胎盘转运的IgG获得被动免疫。基于"卫生假说",早期微生物暴露可降低哮喘风险,但产前微生物暴露或被动免疫是否发挥作用尚不明确。本研究假设:低收入国家出生的母亲因早年微生物暴露更丰富,其胎盘转运给子代的抗菌IgG抗体多样性更高、水平更高,进而保护子代免受哮喘困扰。
技术路线
1、研究人群:纳入波士顿出生队列(BBC)中943对母子,其中64.9%为外国出生母亲(92%来自低收入国家),长期前瞻性随访至儿童期
2、抗体检测:采用PhIP-seq技术与毒力因子抗原库(ToxinScan:涵盖2740个物种、1311个属的14429个毒力因子蛋白),检测脐血中微生物特异性IgG抗体谱
3、结局定义:儿童5岁及以上经医生诊断的哮喘(结合ICD编码),分为"无特应性无哮喘""仅特应性疾病""哮喘(伴或不伴特应性)"三类结局
4、统计分析:采用PERMANOVA分析IgG谱差异,多分类回归模型分析抗体与哮喘风险的关联,中介分析明确抗体的介导作用
主要研究结果
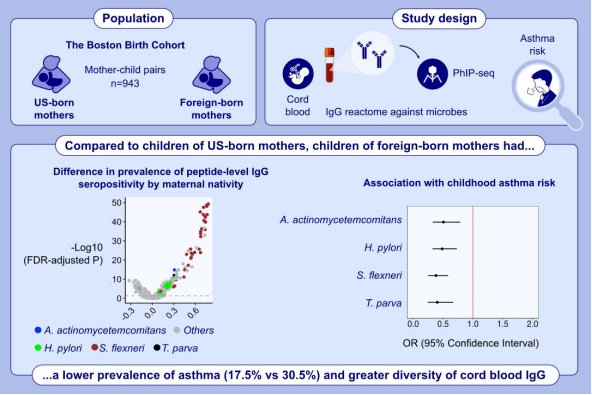
研究人员利用噬菌体免疫沉淀测序(PhIP-seq)技术,检测了波士顿出生队列中943对母子的脐血样本中针对2740种微生物(1311个属)的IgG抗体反应组,探讨母亲出生地、脐血IgG抗体与儿童哮喘及特应性疾病风险的关联。结果显示,母亲出生地方面,外国出生母亲(64.9%,约92%来自低收入/发展中国家)的哮喘患病率(9.3%)显著低于美国出生母亲(19.0%,p<0.001),其子女的哮喘患病率(17.5%)也显著低于美国出生母亲的子女(30.5%,p<0.0001),且定居移民与新移民子女的哮喘率无显著差异(p=0.27)。
脐血IgG抗体谱方面,外国出生母亲的子女脐血中针对数百种微生物的IgG抗体多样性显著更高(FDR<0.05),脐血IgG反应组因母亲出生地不同存在显著差异,可解释7%的变异(R²=0.07,p<0.001),其中弗氏志贺菌(S.flexneri)、刚地弓形虫(T.gondii)等微生物的肽段抗体反应差异尤为明显(Fig.1)。

脐血IgG抗体与儿童哮喘风险的关联方面,在451个随母亲出生地显著变化的肽段中,19个肽段(来自弗氏志贺菌、博伊德氏志贺菌18型、幽门螺杆菌[H.pylori]、小泰勒虫[T.parva]等6种微生物)的血清阳性与儿童哮喘风险呈显著负相关,且血清阳性数量越多,哮喘风险越低(p<0.001),其中弗氏志贺菌ipaC蛋白(残基224-280)肽段的关联最强(OR=0.38,95%CI=0.25-0.58)(Table2;FigureS6);蛋白水平上,4个来自志贺菌属的蛋白血清阳性也与哮喘风险降低显著相关(FDR<0.05)(TableS8),且这些关联在调整母亲哮喘史、母乳喂养、儿童下呼吸道感染史或采用更严格哮喘诊断标准后仍稳健。
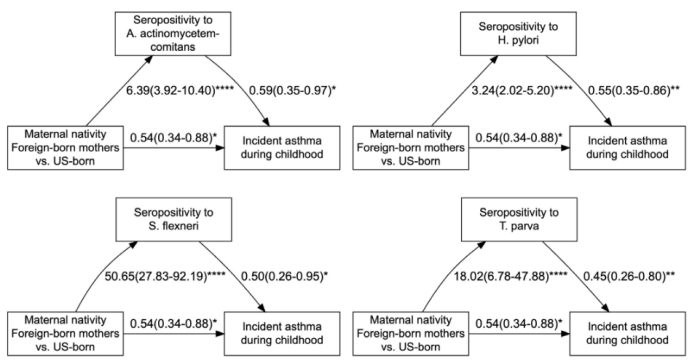
中介效应分析显示,针对伴放线放线杆菌、幽门螺杆菌、弗氏志贺菌和小泰勒虫的脐血IgG血清阳性,分别介导了母亲外国出生状态与儿童哮喘风险负相关关联的19.5%、17.3%、61.8%和25.1%,而2-4种微生物肽段的联合血清阳性可共同解释该关联的33.2%-88.4%(Fig.2)。此外,母亲出生地与儿童“仅特应性疾病”风险无显著关联,未观察到母亲出生地与母亲特应性/哮喘史的显著交互作用。
研究意义与机制探讨
本研究首次证实,母亲早年微生物暴露塑造的抗菌IgG抗体谱,可通过胎盘转运保护子代免受哮喘困扰,部分解释了移民后代哮喘风险较低的现象。其核心机制可能包括:
1.母体IgG调节新生儿免疫发育:在免疫关键窗口期塑造Treg细胞分化,抑制Th2型过敏反应,建立免疫耐受
2. 抑制哮喘相关病原体感染:被动免疫可降低早期下呼吸道感染风险,间接减少哮喘发生
3.符合"卫生假说"的拓展:产前微生物暴露(通过母体抗体)与产后暴露同样具有保护作用
其中,幽门螺杆菌的保护作用与既往研究一致——其vacA毒力因子可诱导免疫耐受;而弗氏志贺菌作为肠道致病菌,其毒力质粒编码的ipa系列蛋白抗体与哮喘风险的强关联,提示肠道-呼吸道免疫轴可能参与哮喘发病机制。
本研究应用的ToxinScan库
本研究采用ToxinScan毒力因子抗原库,涵盖各类致病菌的14429个毒力因子蛋白(包含>17万条肽段),可全面解析针对微生物毒力因子的抗体反应特征,为感染相关免疫研究提供精准工具。
总结
本研究通过大规模前瞻性队列和PhIP-seq高通量技术,揭示了"母亲出生地-胎盘转运抗菌IgG-儿童哮喘风险"的关键关联,证实4种微生物(伴放线放线杆菌、幽门螺杆菌、弗氏志贺菌、小泰勒虫)的特异性IgG抗体是核心保护因子。这一发现不仅深化了对儿童哮喘发病机制的理解,也为哮喘预防提供了新思路——未来可能通过调节母体产前免疫状态或模拟相关抗体效应,开发新型预防策略。后续研究需在其他队列中验证结果,并进一步阐明抗体发挥保护作用的具体分子机制。
如果这篇内容对哮喘研究、免疫流行病学、PhIP-seq技术应用有启发,欢迎分享给同行或团队成员,共同推动儿童过敏性疾病的研究与防控!
参考文献
Hong X, Nadeau KC, Frischmeyer-Guerrerio P, et al. Transplacental antimicrobial antibodies and childhood asthma: Maternal nativity as an upstream factor. Allergy. 2026;81:197–208. https://doi.org/10.1111/all.70167