导语:在癌症免疫治疗领域,免疫检查点抑制剂(CPI)已经成为一种重要的治疗手段。然而,尽管CPI在某些患者中取得了显著的疗效,但其治疗效果在不同患者之间存在显著差异。近年来,科学家们逐渐意识到,除了细胞免疫外,体液免疫(特别是自身抗体)在CPI治疗中也扮演着关键角色。最近发表在《Nature》杂志上的一项研究,通过大规模的自身抗体分析,揭示了体液免疫在CPI治疗中的复杂作用及其对治疗效果的影响。
2025年7月,来自Yale医学院与Fred Hutch的研究团队在近期Nature重磅发表的论文,题为“Humoral determinants of checkpoint immunotherapy”。本研究利用快速细胞外抗原分析技术(REAP),对374名接受CPI治疗的癌症患者和131名健康对照者的血浆样本进行了分析,检测了针对6,172种细胞外和分泌性蛋白(“细胞外蛋白质组”)的自身抗体,首次全面绘制出接受CPI治疗患者的自身抗体谱(autoantibody reactome)进行“自身抗体全关联研究”(AAbWAS,类似全基因组关联研究),揭示了隐藏在体液免疫中的治疗决定因素。

【发表期刊】Nature
【发布时间】2025年7月
【影响因子】55
【核心技术】PhIP-seq
研究背景:
尽管免疫检查点抑制剂(CPI)已显著改善多种癌症患者的生存率,但其疗效差异巨大,缺乏有效预测指标。过去研究多聚焦于T细胞介导的细胞免疫,而体液免疫,尤其是自身抗体(autoantibodies, AAbs)的作用仍知之甚少。考虑到AAbs在多种疾病中可通过中和细胞因子、调节信号通路等方式显著影响免疫功能,作者提出AAbs也可能调控CPI疗效。为系统评估AAbs在癌症免疫治疗中的潜在功能,本研究利用高通量的REAP平台,在374名CPI治疗患者中绘制出外泌蛋白抗体图谱,探索其与疗效及不良反应的关联,旨在揭示新的治疗预测因子和干预靶点。
研究路线

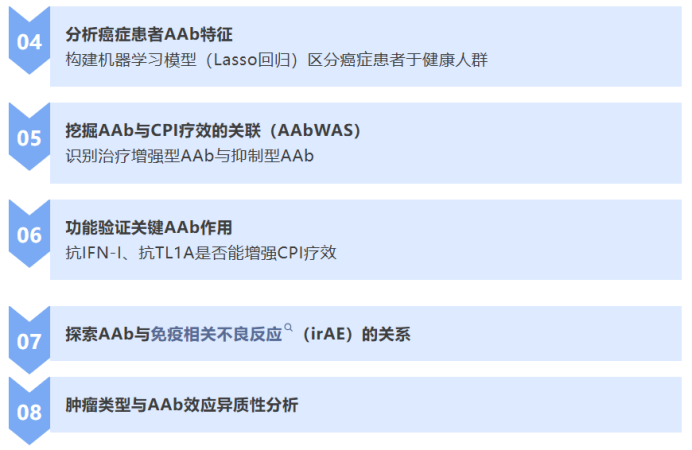
研究亮点抢先看
亮点一:374名癌症患者 × 6172个人类外泌蛋白:研究采用REAP技术,高通量筛查了CPI治疗患者血清中对外泌蛋白的抗体反应,范围涵盖细胞因子、受体、免疫调节因子和肿瘤表面抗原等。
亮点二:自身抗体图谱高度个体化:发现多达2922种独特的自身抗体反应,多数只在极少数个体中出现(<1%),具有高度稀有性和潜在生物功能。
亮点三:抗体图谱可预测治疗响应:某些抗体(如抗IFN-I、抗IL-6、抗TL1A)在CPI治疗响应者中显著富集,甚至具备“治疗增强”作用;而部分抗体如抗BMPR1A/BMPR2则预示疗效不佳。
亮点四:抗IFN-I抗体逆转传统认知:IFN-I通路一向被认为是抗肿瘤的“正面角色”,但研究发现其过度激活反而抑制免疫治疗,携带广泛抗IFN-I抗体的患者几乎全部响应治疗,动物实验也证实了IFN-I阻断能增强CPI效果。
亮点五:TL1A被确认为治疗屏障:另一个新发现是TL1A抗体的保护作用,该因子由肿瘤细胞表达,可诱导CD8+ T细胞凋亡,限制免疫清除。中和TL1A抗体在动物模型中与PD-1抗体联用显著抑制肿瘤生长。
主要研究结果
结果一:自身抗体反应组的多样性
研究团队利用快速细胞外抗原分析技术(REAP),对374名接受CPI治疗的癌症患者和131名健康对照者的血浆样本进行了分析,检测了针对6,172种细胞外和分泌性蛋白的自身抗体。结果显示,癌症患者的自身抗体反应组极为多样化,且与健康个体相比显著增加。尽管这些自身抗体在治疗过程中变化不大,但它们的存在可能对CPI的疗效产生重要影响。
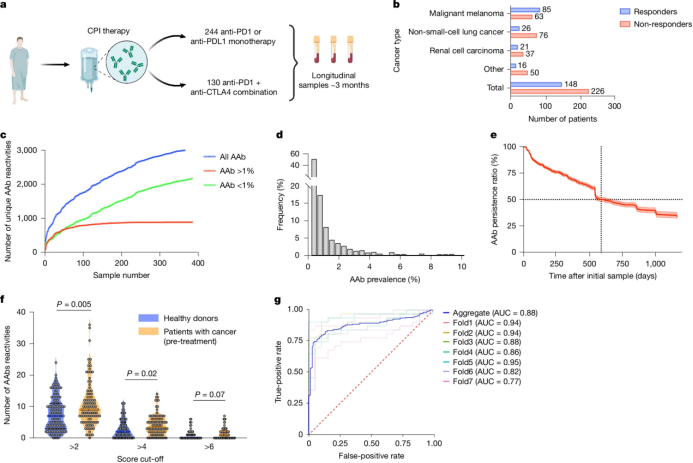
Fig. 1 | Global features of the extracellular AAb reactome in patients treated with CPIs.
结果二:自身抗体与治疗反应的关联
研究发现,针对免疫调节蛋白(如细胞因子、生长因子和免疫受体)的自身抗体与CPI治疗反应显著相关。特别是针对共抑制蛋白(如FGL1、PVRL1、PVRL4和SIRPα)的自身抗体与更好的治疗反应相关,而针对促炎细胞因子(如IL-6、IL-17、OSM)的自身抗体也与更好的治疗反应相关。此外,针对肿瘤相关抗原(如MSLN、MET、GPC1、GPC3)的自身抗体与更好的治疗反应相关,而针对BMPR1A和BMPR2的自身抗体与较差的治疗反应相关。这些自身抗体可能通过中和其靶蛋白的活性来增强或抑制CPI的治疗效果。
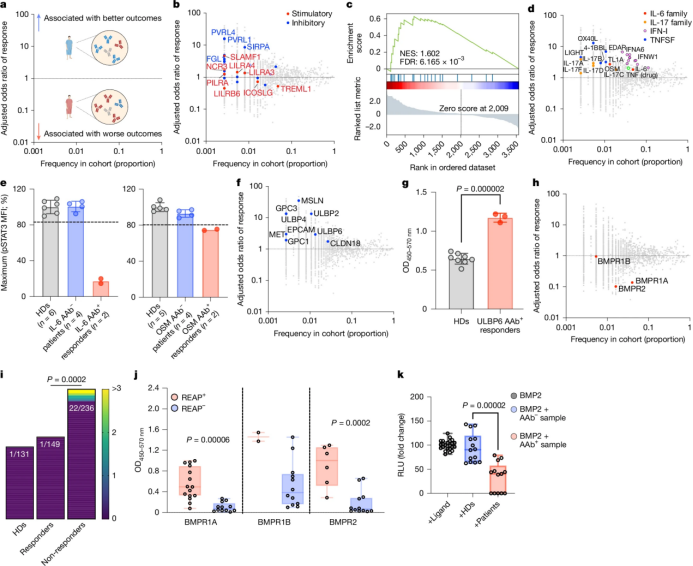
Fig. 2 | Functional AAbs are associated with treatment outcome.
结果三:IFN-I中和自身抗体的作用
针对I型干扰素(IFN-I)家族的自身抗体在CPI治疗反应者中显著富集。这些自身抗体能够中和IFN-I的活性,从而增强CPI的疗效。在小鼠肿瘤模型中,阻断IFN-I信号通路显著增强了CPI的疗效。这表明,IFN-I中和自身抗体可能通过抑制IFN-I的免疫抑制作用来增强CPI的治疗效果。
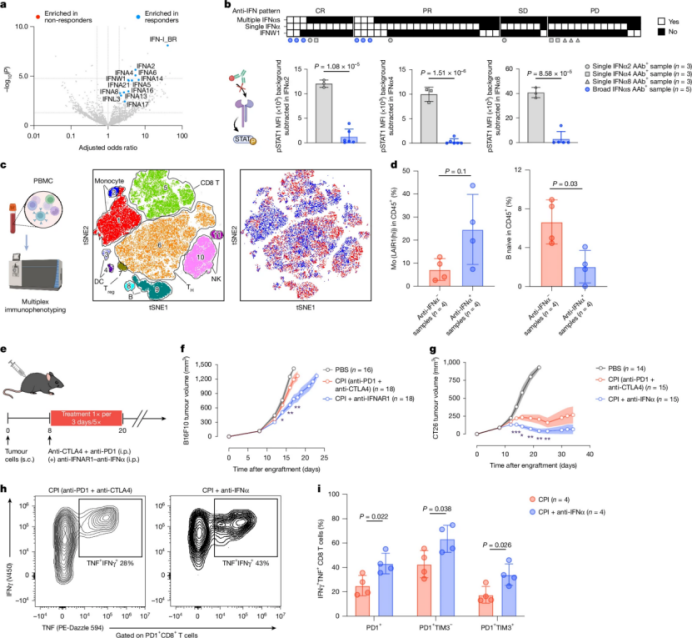
Fig. 3 | Anti-IFN-I AAbs are enriched in CPI responders.
结果四:TL1A自身抗体的作用
针对TNF超家族成员TL1A的自身抗体在CPI治疗反应者中显著富集。这些自身抗体能够抑制TL1A诱导的细胞凋亡,从而增强CPI的疗效。在小鼠肿瘤模型中,联合使用抗TL1A抗体和抗PD1抗体显著增强了抗肿瘤效果。这表明,TL1A自身抗体可能通过抑制TL1A的免疫抑制作用来增强CPI的治疗效果。
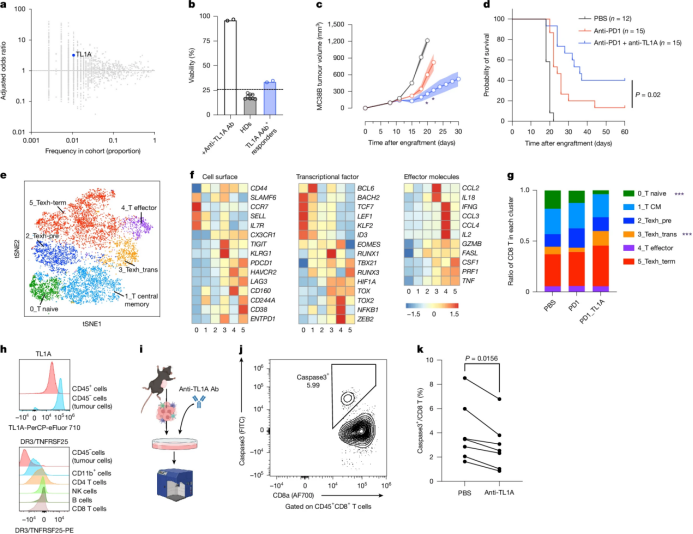
Fig. 4 | Anti-TL1A AAbs are enriched in CPI responders.
结果五:自身抗体与免疫相关不良事件(irAE)的关联
尽管AAb数量与irAE的患病率或严重程度之间没有显著关联,但针对G蛋白偶联受体QRFPR的AAb与垂体炎显著相关。这些AAb在11%的垂体炎患者中被检测到,而在其他irAE患者或健康对照者中未检测到。这表明,某些AAb可能与特定的irAE相关,但总体而言,AAb与irAE之间的关联较为罕见。
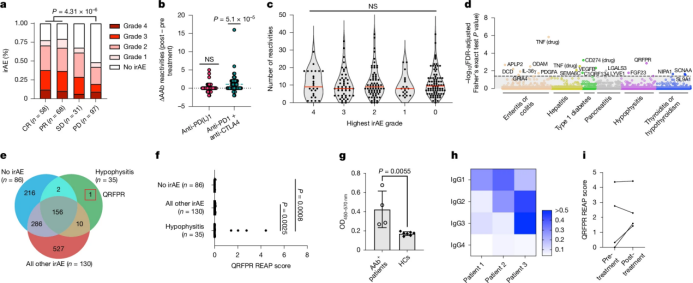
Fig. 5 | Anti-QRFPR AAbs are associated with CPI-induced hypophysitis.
>研究总结
一、自身抗体的临床应用潜力
研究提出了AAb作为生物标志物和治疗靶点的潜力。针对IFN-I和TL1A的AAb可能作为生物标志物,预测CPI治疗的反应。针对这些靶点的药物(如anifrolumab)可能与CPI联合使用,以增强治疗效果。这为开发新的生物标志物和治疗策略提供了潜在的靶点。
二、研究的局限性与未来方向
尽管这项研究提供了许多有价值的发现,但也存在一些局限性。例如,大多数AAb较为罕见,需要更大的队列来检测具有临床相关性的AAb关联。此外,AAb的存在可能并不总是CPI反应的独立因果因素,而是潜在免疫状态的生物标志物。未来的研究需要更大的样本量来验证AAb与CPI治疗反应和irAE之间的关联,并探索其作为生物标志物和治疗靶点的潜力。
参考文献
Dai, Y., Aizenbud, L., Qin, K., Austin, M., Jaycox, J. R., Wang, E. Y., Zhang, L., Fischer, S., Carroll, S. M., Aggelen, H. v., Kluger, Y., Herold, K. C., Furchtgott, L., Kluger, H. M., & Ring, A. M. (2025). Humoral determinants of checkpoint immunotherapy. Nature.